Termodünaamika
Termodünaamika (inglise keeles thermodynamcs) uurib soojusnähtusi, soojusvoogude liikumist ja energia üleminekuid ühest vormist teise. Katsed algasid juba 19.sajandil selleks, et teada saada kuidas toimivad maailmas soojus ja energia, katse tulemustest tuletasid nad seaduseid. Termodünaamikal on kolm seadust. Termodünaamika esimene seadus väidab, et energia ei saa tekkida ega hävida ehk energia muundub ühest liigist teise. Termodünaamika teine sedaus vädab, et kõigis looduslikes protsessides entroopia kavab ehk lihtsamalt öeldses soojus liigub kuumemast kohast külmemasse. Termodünaamika kolmas seadus ütleb, et on olemas minimaalne temperatuur, mida nimetakse absoluutseks nulliks ehk sellel temperatuuril on ainel minimaalne võimalik soojusenergia ja ta ei saa muutuda külmemaks. Celsiuse skaala järgi on absoluutne null -273,15 kraadi ja Kelvini skaala järgi 0K.
Ideaalne gaas
Ideaalne gaas on reaalse gaasi lihtsaim mudel, selle osakesed ei ole omavahel mingis vastastik mõjus ning nende mõõtmed võib jätta arvestamata. Ükski reaalne gaas ei ole ideaalne gaas. Ideaalse gaasi lõhna levimise kiirus on 450 m/s, kuid reaalsel gaasil vaid mõnikümmned cm/s. Nagu juba eelnevalt mainitud, siis ideaalsel gaasil ei ole molekulide vahel mitte mingit vastastikmõjus, kuid reaalse gaasi molekulid on omavahel vastastikmõjus. Ideaalset gaasi on võimalik lõpmatuseni kokkusuruda, kuid reaalselt pole see võimalik. Ideaalset gaasi pole võimalik veeldada, kuid reaalselt gaasi on võimalik. Väga hõre reaalne gaas ja ideaalne gaas on väga sarnased.
Isoprotsessid
Gaassidel on kolm põhilist termodünaamilist parameetrit, milleks on rõhk, ruumala ja temperatuur. Olemas on kolm erinevat isoprotsessi - isobaarne, isohoorne ja isotermne. Igas isoprotsessis on erinev parameeter konstatne.
Isobaarne
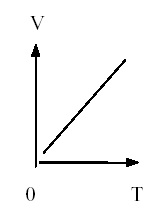
Isobaarses protsessis on konstantseks suuruseks rõhk. See on paika pandud Gay-Lussaci seadusega ning selle sõnastus oleks järgmine: jääval rõhul on gaasi ruumala ja temperatuur võrdelises sõltuvuses.
Isohoorne
Isohoorses protsessis on konstantseks suuruseks ruumala. See on määratletud Charlesi seadusega ning selle sõnastus oleks järgmine: jääval ruumalal on rõhk ja temperatuur võrdelises sõltuvuses.
Isotermne
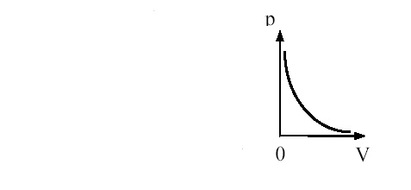
Isotermses protsessi on konstantseks suuruseks temperatuur. See on määratletud Boyle-Mariotte seadusega ning selle sõnastus oleks järgmine: jääval temperatuuril on rõhk ja ruumala võrdelises sõltuvuses.
Külmkapp
Külmkapi tööpõhimõte on külma tootmine. Külmkapp võtab toiduainetest sooja ära külmaandja ehk aurusti abiga ja eraldab sooja keskkonda kondensaatori abiga. Kogu külmutamine toimub külmkapis teatud gaasi ringiajamise abil. Kõigepealt satub vaadeldav gaas kompressorisse, kus see vedelikuks muudetakse. Selle tulemusena tõuseb nii gaasi rõhk kui ka temperatuur. Edasi liigub gaas torudesse, mis paiknevad väljaspool külmkappi, harilikult kapi tagaküljel. Neis torudes liikudes annab gaas ära osa soojusest ja kondenseerub vedelikuks. Edasi liigub see nüüd-juba-vedelik spetsiaalsesse ventiili, mille abil lastakse suure rõhu all oleval vedelikul voolata madala rõhuga piirkonda. Selle tulemusena toimub paisumistöö, suure rõhu all olev vedelik aurustub ja jahtub. See jahe gaas juhitaksegi külmiku sisse ja see, mis külmikus toimub, ongi lihtsalt temperatuuride ühtlustumine. Edasi liigub gaas jälle kompressorisse ja kõik hakkab otsast peale. Tavaliselt kasutatakse külmikutes selle tsüklis oleva gaasina freooni, harvemini ka ammoniaaki või teisi gaase. Samuti ei tööta see gaasitsükkel külmkapis kogu aeg.
Soojuspump
Soojuspump pumpab soojusenergiat ühest piirkonnast teise. Soojuspumba tööpõhimõte on ümbritsevast keskkonnast (õhust, maapinnast või veekogust) soojuse ammutamine ja teatud ainete (enamasti freooni) füüsikalisi omadusi ja elektrienergiat kasutades, tõsta (pumbata) soojakandja aine temperatuur tasemele, kus seda saab kasutada hoonete kütmiseks ja sooja tarbevee valmistamiseks. See on põhimõtteliselt sama protsess, mis toimub külmikute juures. Kui külmikute juures on eesmärgiks temperatuuri alandamine, on soojuspumba juures eesmärgiks temperatuuri tõstmine. See protsess on pööratav ja soojuspumpasid saabki külmal aastaajal kasutada kütmiseks.
Soojuspumba tööprotsess koosneb tinglikult neljast osast.
1. Soojuse absorbeerimine keskkonnast. Madal rõhk
Seda ülesannet täidab aurusti (1). Madala temperatuuriga ja rõhuga külmaagens kulgeb läbi aurusti ja soojeneb. Aurusti saab energiat soojusülekande teel (õhu temperatuur on tunduvalt kõrgem külmaagensi temperatuurist) ja õhu niiskuse kondenseerumisest aurusti pinnale.
2. Külmaagensi temperatuuri tõstmine. Kõrge rõhk
Seda teeb kompressor (2). Külmaagensi kokkusurumisega tõuseb nii selle temperatuur kui ka kondenseerumispunkti temperatuur.
3. Soojuse ülekanne tarbivale keskkonnale. Kõrge rõhk
Kõrge temperatuuriga külmaagens kulgeb läbi soojusvaheti (kondensori) (3), kus ta annab soojuse kütteveele kõigepealt soojusülekande teel, millele lisandub vabanev energiahulk külmaagensi kondenseerumisest.
4. Rõhu alandamine. Madal rõhk
Kondenseerunud külmaagens juhitakse läbi paisuventiili, kus rõhk ja temperatuur langevad protsessi algsele tasemele
Entroopia
Entroopia on termodünaamiline funktsioon, mis iseloomustab süsteemi liikumist (püüdlemist)
korrapäratuse poole. Entroopia on energia hajumise, ehk lihtsamalt kaduvuse mõõt. Entroopia on deemonlik parameeter. Sellise protsesside ühesuunalisuse musternäiteks on kuuma keha (esimese keha) jahtumine, temalt soojuse ülekandumine külmemale naaberkehale (teisele kehale) ilma et see soojus edaspidi iseeneslikult teiselt kehalt jälle esimesele tagasi läheks. Mis läinud, see läinud, ütleb parastavalt entroopia. Entroopia väärtus on muidugi selle protsessi tagajärjel järjekordselt suurenenud.
Elusolend kui soojusmasin
Bioloogilised olendid ei kasuta töö tegemiseks gaasi paisumist, vaid lihasvalkude potensiaalset energiat. Elusolendid saavad oma energiat toidust. Ka bioloogile olend eraldab väliskeskkonda soojust.